Лекція 4. Сучасні методи дослідження стану навколишнього середовища (2 год)
2. Методи розділення та концентрування складних речовин
Доцільно відмітити, що в хімічному аналізі широко застосовують різні методи розділення складних сумішей речовин та концентрування речовин, які передують проведенню аналізу. Для цього використовують, наприклад, перегонку, маскування йонів і дрібне осадження, хроматографію, екстракцію, адсорбцію тощо.
Маскування звичайно проводять зв’язуванням заважаючи йонів у комплексні сполуки – флуоридні (Fe3+, Al3+), хлоридні (Ag+ , Fe3+, Mn2+), тіоціанатні, аміачні, тартратні і деякі інші. Реагент, який застосовують для аналізу, повинен утворювати із досліджуваною речовиною значно міцнішу сполуку, ніж маскуючий реагент.
Видалення заважаючих йонів в осад. Заважаючи йони осаджують у вигляді карбонатів, гідроксидів, сульфідів, фосфатів, хроматів. Для цього підбирають осаджувач для утворення осаду із малим значенням добутку розчинності (менше 10-10 -10-12).
Екстракція органічними розчинниками. Застосовується для видалення, головним чином, речовин здатних до комплексоутворення. Частіше за все використовують екстракцію хлоридних, дитизонатних, оксіхінолятних комплексів. Нейтральні комплекси багатьох метал-йонів добре розчинні в органічних розчинниках. Це дозволяє видалити заважаючі йони, якщо додати необхідний комплексоутворювач і органічний розчинник, який не змішується з водою (наприклад, хлороформ). Комплекс, який утворюється, переходить в органічний розчинник і видаляється із водної фази.
Окиснення і відновлення речовин. Ці реакції використовуються в тих випадках, коли заважаючи йони здатні окислюватися або відновлюватися. Таким способом, наприклад, видаляють Сr 3+ (окиснення до СrO42-), Mn2+ (окиснення до MnO4- ), Ві2+ (відновлення до Ві0 ) та інші йони.
Адсорбція. Адсорбцією називають поглинання речовин із газового або рідкого середовища поверхневим шаром твердого тіла – адсорбенту. Адсорбцію відрізняють від абсорбції – поглинання речовин усім об’ємом абсорбенту, наприклад, поглинання аміаку водою. При молекулярній адсорбції речовина приєднується до поверхні адсорбенту завдяки:
а) електростатичного (диполь-дипольного або йон-дипольного) притягання молекул речовин до заряджених ділянок поверхні адсорбенту;
б) за допомогою водневих зв’язків.
При хемосорбції речовина вступає в хімічну реакцію з поверхнею адсорбенту. Частіше всього це – реакція обміну йонами між адсорбентом і розчином – так звана йонообмінна адсорбція.
Екстракція. Вибіркове розчинення окремих компонентів суміші речовин в будь-якому розчиннику називають екстракцією. Розрізняють екстракцію в системі тверда речовина – рідина (із твердих тіл) і в системі рідина – рідина (із розчинів речовин). Екстракція із твердих тіл. Застосовують для вибіркового розчинення одного або кількох компонентів твердих матеріалів (руд, сплавів, рослинної сировини). Твердий матеріал попередньо підсушують (якщо необхідно), подрібнюють і вводять в контакт із розчинником, який найбільше підходить – екстрагентом. Екстрагент проводить вибіркове розчинення певних компонентів матеріалу. Потім відокремлюють отриманий розчин компонентів – екстрат, і проводять його аналіз. Для отримання правильних результатів аналізу необхідно, щоб екстрагент повністю проекстрагував досліджувані речовини.
Екстракцію проводять екстрагентами, які добре розчиняють певні речовини. Для екстракції мінеральних речовин застосовують воду, розчини кислот або лугів, здійснюючи при цьому переведення мінеральних речовин у розчинну форму.
Рідинна екстракція. Застосовують для вибіркового вилучення речовин із водних розчинів за допомогою органічного розчинника, який не змішується з водою (хлороформ СНСl3, бензол С6Н6 та інші). Використовують два види рідинної екстракції – з хімічною реакцією і без неї. У першому випадку водний розчин речовин обробляють будь-яким реагентом, отримуючи сполуки, які добре розчинні в органічних розчинниках. Частіше за все для цього використовують добування комплексних сполук (хелатів), добре розчинних в органічних розчинниках. Такими властивостями володіють, наприклад, оксихіноляти, дитізонати, тіоціанати катіонів металів. При екстракції без хімічної реакції використовують здатність деяких речовин розчинятись у воді і органічних розчинниках (СН3СООН, Н2SO4, FeCl3, фенол та інші).
Якщо екстракції підлягають декілька речовин, то внаслідок різної їхньої здатності до розподілу між фазами проходить їх часткове розділення. Таким чином, застосовуючи рідинну екстракцію, можна розділити речовини. Часто для збільшення повноти розділення використовують багатоступінчасту екстракцію, для чого добутий екстракт (наприклад, Н2SO4 і НСООН) вводять у новий контакт з водою, екстрагуючи із органічної фази у водну частину речовин і т. д. При цьому розділення покращується. Для проведення рідинної екстракції звичайно використовують ділильні лійки або спеціальні апарати. Процес ведуть при помішуванні
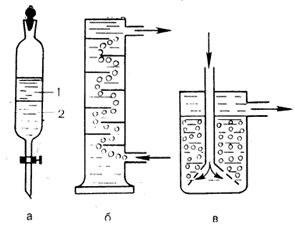
Рис. 1. Прилади для рідинної екстракції: а – ділильна лійка; 1 – органічна фаза; 2 – водна фаза; б – екстракційна колонка; в – апарат із перфорованою лійкою
Перегонка. Багато речовини досить леткі і можуть бути виділені із матеріалу методом аналітичної перегонки (або дистиляції), яка ґрунтується на випаровуванні і конденсації летких компонентів.
Аналітичну перегонку застосовують для відділення і кількісного визначення летких ефірних масел (в рослинній сировині), оцтової кислоти, етилового спирту. Цим методом визначають ацетильні групи (СН3СОО– ) і нітроген в органічних сполуках.
Хроматографія. Метод хроматографії широко застосовують для розділення і аналізу складних сумішей речовин. В основі цього аналізу лежать сорбційні процеси, розподіл речовин між двома фазами і явища осадження. У відповідності з процесами, що лежать в основі методу, розрізняють адсорбційну, розподільну і осадову хроматографію.
Адсорбційна хроматографія. В цьому методі застосовують спеціальні речовини з добре розвинутою поверхнею – адсорбенти, які здатні утримувати на своїй поверхні з різною силою хімічні речовини, як за допомогою хімічного зв’язку, так і за допомогою молекулярних сил і поверхневих явищ.
Йонообмінна хроматографія. Деякі адсорбенти здатні до обміну своїх йонів на йони електроліту з розчину. Такі сорбенти називають йонітами. Йоніти, які здатні обмінювати свої катіони на катіони електроліту, що містяться в розчині, називаються катіонітами; йоніти, які здатні до обміну своїх аніонів, називаються аніонітами. В якості йонообмінних адсорбентів використовують природні і штучні алюмосилікати (бентоніт, цеоліт, польовий шпат, пермутит), а також синтетичні неорганічні йоніти - оксиди і гідроксиди алюмінію, хрому, олова, силікагель, фосформолібдати та органічні смоли – продукти конденсації фенолів із формальдегідом. Смоли являють собою різного роду пластичні маси і називають органолітами.
Процес хроматографії проводять у хроматографічній колонці, яка заповнена адсорбентом. Розподільна хроматографія. Ґрунтується на здатності речовини розподілятись між двома фазами, які не змішуються при русі одна відносно одної. В залежності від участі в процесі фаз розрізняють газорідинну і рідинну хроматографію. У випадку газорідинної хроматографії використовується здатність речовин знаходитись у газоподібному стані в газовій фазі і у розчиненому стані в рідині. Нерухомою фазою служить рідина, яка нанесена на тверду фазу - носій, або стінки капілярної трубки, рухомий - газ, який проходить через шар адсорбенту або капілярні трубки. Робоча колонка в цьому методі поміщається в термостат і нагрівається до 200 – 400 0 С. Проба речовини вноситься в потік газу, випаровується і разом з потоком газу рухається через колонку, де розділяється на індивідуальні речовини. При виході із колонки спеціальні детектори реєструють присутність речовини і подають сигнал на самописець. За місцем розміщення сигналу, який на хроматограмі має вигляд піка, роблять висновок про наявність у суміші тієї чи іншої речовини. Величина площі піку дозволяє зробити висновок про кількість речовини. Цей метод має високу чутливість і вибірковість і знайшов широке застосування при аналізі суміші летких органічних сполук. З усіх видів розподільної хроматографії найширше застосування знайшли колоночна, паперова і тонкошарова хроматографії.
Рідина–рідинна хроматографія. Розділення речовин проходить внаслідок їх різної здатності розділятися між двома рідкими фазами. При контакті двох фаз наступає рівновага, при якій в кожній фазі містяться певні концентрації речовини. При русі однієї фази відносно іншої рівновага порушується і речовина переходить із нерухомої у рухому фазу, вільну від речовини, і навпаки. Суміш речовин при цьому розділяється. В якості нерухомої рідкої фази (хроматографічний шар) використовують пористі матеріали з великою поверхнею, які змочені будь - якою рідиною (часто водою). В якості рухомої фази використовують суміші різних органічних розчинників.
Колоночна хроматографія. Проводять на колонці зі скла, яка заповнена адсорбентом (оксид алюмінію, силікагель та ін.), на який наносять попередньо нерухому рідку фазу. В колонку вносять 0,2-0,5 см3 розчину суміші речовин і потім через неї пропускають рухому фазу і розчин детектуючих (ті, що виявляють) реагентів. Так, для виявлення Fe3+ застосовують розчин амонію тіоціанат, Ni2+ – розчин діацетилдиоксиму, Сu2+ – розчин амоніаку. Рухома фаза проводить розділення йонів, розчин реагенту детектує зони, де знаходяться виявлені йони.
Паперова хроматографія. Ґрунтується на рухові розчинника на спеціальному папері. Якщо кювета з розчинником знаходиться внизу і розчинник рухається по паперу вгору, метод називається висхідною паперовою хроматографією; при рухові розчинника згори до низу – низхідною паперовою хроматографією. Паперова хроматографія проводиться на спеціальному хроматографічному папері. Нерухомою фазою служить волога, яка знаходиться на волокнах паперу, рухомою – розчинник. На смужці паперу помічають стартову лінію, на яку наносять невелику кількість (1–2 каплі) дослідного розчину суміші речовин і стандартів (міток). Підсушують нанесені каплі і занурюють нижній край стрічки паперу в кювету з розчинником, яка поміщена в герметично закриту хроматографічну камеру, попередньо насичену парами розчинника. Це необхідно для попередження випаровування розчинника з паперу. Внаслідок капілярних сил розчинник піднімається по смужці паперу, ділячи суміш на плями індивідуальних речовин. Хроматографію ведуть до тих пір, доки розчинник не пройде 20– 25 см. Смужку підсушують на повітрі і збризкують розчином проявника. Речовини при цьому проявляються у вигляді плям, які забарвлені у різні кольори.
Тонкошарова хроматографія. Проводиться аналогічно паперовій. Тут використовують або готові пластинки із закріпленим шаром сорбенту на фользі або готують тонкий шар сорбенту (силікагель, алюмінію оксид) на скляних пластинках (від скляних негативів).
Осадова хроматографія. Ґрунтується на утворенні осадів речовин з реагентами і різній їх розчинності у розчиннику, який рухається на фільтрувальному чи хроматографічному папері. На папір наносять декілька капель розчину речовини, потім додають розчин реактиву і одержані кольорові осади розганяють током розчинника.
Електрохроматографія, або електрофорез на папері. Ґрунтується на здатності йонів рухатись у розчині під дією електричного поля високої напруги (400–600 В). При цьому катіони рухаються до катоду, аніони - до аноду. Різні йони відрізняються один від одного рухомістю, зарядом і в електричному полі рухаються з різною швидкістю, внаслідок чого проходить їх розділення. Електрофорез проводять у буферному розчині, яким змочують для кращої провідності струму папір, який поміщають у камеру для електрофорезу.
Шрифти
Розмір шрифта
Колір тексту
Колір тла
Кернінг шрифтів
Видимість картинок
Інтервал між літерами
Висота рядка
Виділити посилання
Вирівнювання тексту
Ширина абзацу